Sportherz – auch ein starker Motor kann stottern
Der Herzmuskel kann sich durch intensiven, langjährigen (Ausdauer-)Sport strukturell und funktionell an die Belastung anpassen. Das Gewicht steigt, das Herzvolumen erhöht sich ebenso wie das Schlagvolumen und die Sauerstoffaufnahmekapazität. Klassischerweise zeichnet sich ein Sportherz durch eine harmonische Vergrößerung aller vier Herzkammern aus. Ein Mindestumfang von mehr als sieben Stunden intensivem bis hochintensivem Ausdauertraining pro Woche über Monate und Jahre ist hierfür nötig.
Die vorherrschende Expertenmeinung geht davon aus, dass es kein Kraftsportherz gibt, also dass selbst hochintensiv betriebener Kraftsport nicht zu den genannten Anpassungen der exzentrischen Hypertrophie führt. Die typischen Sportherz-Kandidaten sind daher Ausdauerathleten wie Skilangläufer, Langstreckenläufer, Triathleten, Radfahrer, aber auch Handballer.
Physiologisch oder pathologisch – das ist hier die Frage
Ob Anpassungen noch physiologisch oder schon pathologisch sind, ist nicht immer leicht zu beurteilen, da die Variabilität sehr groß ist – selbst Spitzensportler können ein normal kleines Herz haben. Auch sind Anpassungen möglich, die bestimmten Krankheitsbildern im Anfangsstadium ähneln, etwa einer dilatativen oder hypertrophen Kardiomyopathie. »Wir können häufig nur mit Wahrscheinlichkeiten arbeiten und trotz umfangreicher Diagnostik bleibt manchmal eine Restunsicherheit«, erklärt Prof. Dr. Christof Burgstahler, Facharzt für Innere Medizin, Kardiologie und Sportmedizin am Universitätsklinikum Tübingen.
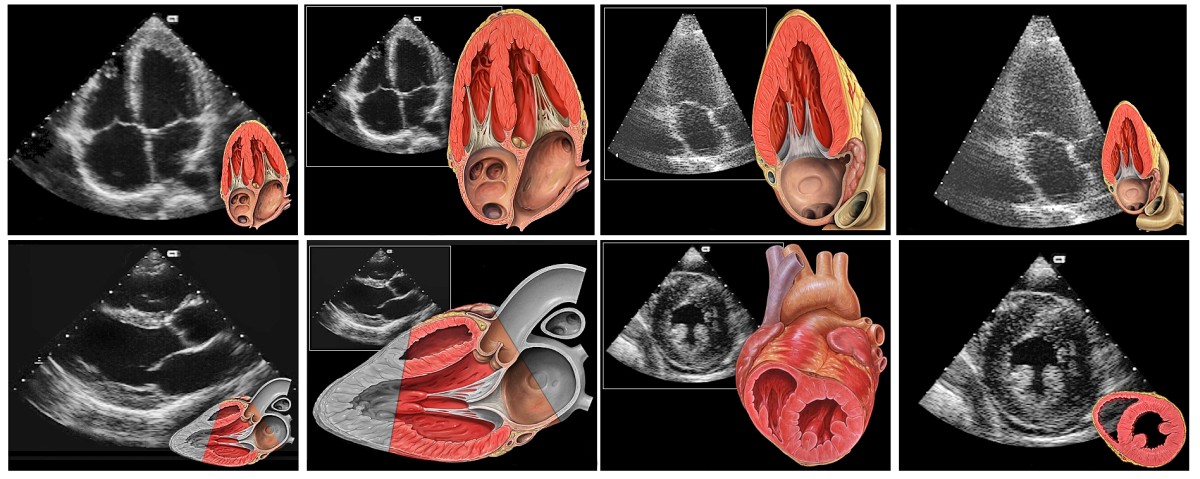
Eine solche Untersuchungsroutine umfasst neben der Familien- und Sportanamnese das Ruhe- und Belastungs-EKG, eine Echokardiographie sowie gegebenenfalls weiterführende Diagnostik wie CT, MRT, klinische Laborparameter oder genetische Diagnostik. Manchmal bleibt nur, den Verlauf über mehrere Jahre zu beobachten. Alternativ – und bei Sportlern verständlicherweise wenig beliebt – kann über eine Sportpause von drei bis sechs Monaten beobachtet werden, ob Rückbildungsprozesse stattfinden, wie sie für ein antrainiertes Sportherz typisch wären. Doch selbst diese Erkenntnisse müssen nicht eindeutig sein.
Theorien besagen nämlich, dass es auch Menschen mit physiologisch größeren Herzen gibt – genauso wie Sportler, die kein Sportherz ausbilden. Frau Dr. Hasema Persch ist Leiterin der Ambulanz der Sport- und Rehabilitationsmedizin der Uniklinik Ulm. Sie ergänzt: »Bei Unklarheiten kann auch eine Spiroergometrie weitere Hinweise darauf geben, ob Veränderungen durch eine überdurchschnittliche Leistungsfähigkeit bedingt sein können. Auch die Pumpleistung muss beim gesunden Athleten in Ruhe echokardiographisch über 50 Prozent liegen.«
Prof. Burgstahler betont: »Man kann sich eben nicht darauf verlassen, dass jemand, der sehr leistungsfähig ist, nicht auch herzkrank sein kann.« Manchen Athleten wird eventuell über viele Jahre ein Sportherz attestiert, während sie in Wahrheit unter einer Herzerkrankung leiden. Auch weil die Prävalenz von kardiologischen Erkrankungen im Alter zunimmt, wird empfohlen, nach längerer Sportpause eine sportmedizinische Untersuchung inklusive Belastungs-EKG durchführen zu lassen. Die DGSP empfiehlt sie für Sportler ab dem 35. Lebensjahr. »Grundsätzlich abgeklärt werden müssen Veränderungen wie eine ungewöhnliche Veränderung nur einer Herzkammer, insbesondere eine asymmetrische linksventrikuläre Hypertrophie und Kontraktilitäts- bzw. Wandbewegungsstörungen sowie eine dilatierte Aorta ascendens«, erklärt Dr. Persch.

Nächste Seite: EKG-Veränderungen beim Sportler: die Seattle-Kriterien | Damoklesschwert Myokarditis
EKG-Veränderungen beim Sportler: die Seattle-Kriterien
Das Ruhe-EKG eines Athleten kann ebenfalls Anlass zur Unsicherheit bieten: »Etwa 60 Prozent aller Athleten haben kein vollständig normales EKG. Bei ca. 80 Prozent werden Sinusbradykardien zwischen 31 und 50 Schlägen pro Minute beobachtet, bei ca. 55 Prozent Sinusarrythmien und bei bis zu 8 Prozent wechselnde Vorhoferregungen in Ruhe. »Da ist es nicht immer einfach zu beurteilen, was noch gesund ist«, erklärt Prof. Dr. Matthias Antz, leitender Abteilungsarzt der Elektrophysiologie am Klinikum Braunschweig.
Da viele Veränderungen beim Sportler deutlich häufiger auftreten als in der Allgemeinbevölkerung, außerdem von der Ethnizität abhängen (Unterschiede zwischen Sportlern kaukasischer und afrikanischer/karibischer Abstammung) und zugleich nicht zwingend pathologisch sind, wurden im Jahr 2012 die Seattle-Kriterien entwickelt. Sie geben Hinweise darauf, welche Veränderungen im EKG bei Athleten noch normal sind und welche nicht mehr. Dazu zählen neben den genannten beispielsweise auch AV-Block 1. Grades und AV-Block 2. Grades Typ Wenckebach, ein inkompletter Rechtsschenkelblock (bei bis zu 40 Prozent) und weitere (2).
»Eine Ursache der Anpassungen liegt in der starken Erregung des vagalen Nervensystems beim Athleten. Sowohl die Aktivität des Sinus- als auch des AV-Knotens wird dadurch verändert«, erklärt Prof. Antz. Eine weitere Ursache liegt in den muskulären Adaptationen an das intensive Training. »Besonders das rechte Herz wird stark beansprucht, was zum so genannten Remodelling, also einer Vergrößerung des rechten Herzens, und damit zu veränderten Leitungszeiten führen kann«, so der Elektrophysiologe weiter. Dass intensiver Sport nicht nur gesund ist, zeigt sich auch beim Vorhofflimmern. Marathonläufer, Radsportler oder Langläufer haben ein bis zu zehnfach höheres Risiko als ein Freizeitsportler, der täglich »nur« sechs Kilometer joggt. Werden die Trainingsumfänge und die Trainingsintensität reduziert, kann sich die Situation normalisieren.
Damoklesschwert Myokarditis
Noch immer ist nicht vollständig entschlüsselt, unter welchen Umständen es zu einer Herzmuskelentzündung kommt. Eine Kombination aus einem Infekt, wahrscheinlich mit Fieber, und nicht ausreichender körperlicher Schonung scheint dafür häufig verantwortlich zu sein. Doch nicht bei jedem Infekt und bei jedem Sportler tritt eine Myokarditis auf und auch die Bandbreite des klinischen Bildes ist groß: von asymptomatischen bis zu schweren Verläufen, die eine Herztransplantation notwendig machen, ist alles möglich. Auch der eindeutige Nachweis, ob der Herzmuskel entzündet ist oder war, ist nicht in jedem Fall möglich.
»Es gibt Fälle, in denen wir trotz umfangreicher Diagnostik nicht abschließend sagen können, ob eine Myokarditis vorliegt«, erklärt Prof. Burgstahler. Möglicherweise hängt die Ausprägung mit der Art des Erregers statt, der die ursprüngliche Infektion ausgelöst hat. Da eine Myokarditis das Risiko für einen plötzlichen Herztod massiv erhöht, ist es notwendig, diese komplett auszukurieren. »Das Problem ist, dass es keine Evidenz dafür gibt, wie lange Athleten mit dem Sport pausieren sollen. Eine Konsensempfehlung geht von mindestens drei bis sechs Monaten aus«, führt der Kardiologe aus. Um auf bessere Daten zurückgreifen zu können, wurde an der Uniklinik Tübingen ein Register angelegt, das Sportler mit vermeintlicher oder gesicherter Myokarditis beobachtet und betreut (4). Bei den bisher begleiteten Athleten gab es bislang keine fatalen Ereignisse. Wann aus den Daten konkrete Empfehlungen abgeleitet werden können, ist noch offen.

Nächste Seite: Sportkardiologisches Screening – Stärken und Schwächen
Sportkardiologisches Screening – Stärken und Schwächen
Generell ist bekannt, dass ein erhöhtes kardiovaskuläres Risiko besteht, während das Herz-Kreislauf-System beansprucht wird: Für einen Myokardinfarkt ist es während körperlicher Aktivität um das Zwei- bis Sechsfache höher als in Ruhe, für einen plötzlichen Herztod um das 17-Fache (5). Bei Athleten unter 35 Jahren ist die hypertrophe Kardiomyopathie eine der häufigsten Ursachen, und die Myokarditis trägt ebenfalls nicht unerheblich zu den Fallzahlen bei. Rückwirkend betrachtet zeigten viele Patienten mit überlebtem plötzlichem Herzstillstand oder plötzlichem Herztod Symptome oder Anzeichen, die hätten erkannt werden können.
Daher gibt es eine anhaltende Diskussion um Sinn, Notwendigkeit und Wirtschaftlichkeit eines sportkardiologischen Screenings. Unverzichtbar, sagen die einen und berufen sich auf die Einführung einer verpflichtenden Screeninguntersuchung bei Leistungssportlern in der Region Venetien in Italien. Dort konnte die Inzidenz des Herztods um 89 Prozent gesenkt werden, wobei die in dieser Region häufig vorkommenden Ionenkanalerkrankungen via EKG gut detektierbar sind. Wie effektiv das Screening daher an einem anderen Kollektiv wäre, kann nicht genau gesagt werden.
Screenings seien überflüssig, sagen andere und betonen den hohen wirtschaftlichen Aufwand, der notwendig wäre, um die 0,2 bis 0,7 Prozent der Betroffenen mit potenziell tödlichen Herzerkrankungen zu finden. Auch falsch positive Befunde, die unter anderem durch mangelnde Erfahrung eines Beurteilenden verursacht werden können und für Verunsicherung beim Athleten sorgen, werden als Argument angeführt. Dass hier Fortbildung helfen kann, haben NR Riding und JA Drezner in einer aktuellen Untersuchung gezeigt.
An einer Online-Schulung zur Interpretation von Sportler-EKGs nahmen mehr als 10 000 Mitarbeiter unterschiedlicher medizinischer Berufsgruppen teil – von Krankenschwestern bis Kardiologen. Zu Beginn des Kurses war das Wissen sehr unterschiedlich; Kardiologen schnitten mit 83 Prozent richtigen Beurteilungen am besten ab. Am Ende des Kurses hatten sich fast alle Berufsgruppen deutlich verbessert. Einige, wie beispielsweise Krankenschwestern und -pfleger in der Kardiologie, Sportmediziner und Notfallmediziner stellten dann sogar die Kardiologen in den Schatten (6).
Neben einem möglichen Screening der Athleten haben sich aber noch andere Methoden als hocheffektiv erwiesen. Wurden in einer Studie Trainer über das mögliche Auftreten und die Symptome eines Herz-Kreislauf-Stillstandes aufgeklärt und in Wiederbelebungsmaßnahmen geschult, überlebten 83 Prozent der Athleten. Befand sich an der Sportstätte ein automatischer Defibrillator, so stieg die Rate auf 89 Prozent (3), in einer anderen Studie sogar auf 93 Prozent (1).
Eine nicht zu unterschätzende Ursache für kardiovaskuläre Symptome und Befunde beim Sportler ist Doping bzw. Arzneimittelmissbrauch. Die klinischen Hinweise auf Medikamentenmissbrauch sollten nicht übersehen werden – auch und besonders beim ambitionierten Breitensportler.
■ Hutterer C
Ähnliche Beiträge zum Thema finden Sie weiter unten!
Quellen:
Aschieri D, Penela D, Pelizzoni V, Guerra F, Vermi AC, Rossi L, Torretta L, Losi G, Villani GQ, Capucci A. Outcomes after sudden cardiac arrest in sports centres with and without on-site external defibrillators. Heart. 2018; 104: 1344-1349. doi:10.1136/heartjnl-2017-312441
Drezner JA, Ackerman MJ, Anderson J, Ashley E, Asplund CA, Baggish AL, Börjesson M, Cannon BC, Corrado D, DiFiori JP, Fischbach P, Froelicher V, Harmon KG, Heidbuchel H, Marek J, Owens DS, Paul S, Pelliccia A, Prutkin JM, Salerno JC, Schmied CM, Sharma S, Stein R, Vetter VL, Wilson MG. Electrocardiographic interpretation in athletes: the 'Seattle criteria'. Br J Sports Med. 2013; 47: 122-4. doi:10.1136/bjsports-2012-092067
Drezner JA, Peterson DF, Siebert DM, Thomas LC, Lopez-Anderson M, Suchsland MZ, Harmon KG, Kucera KL. Survival After Exercise-Related Sudden Cardiac Arrest in Young Athletes: Can We Do Better? Sports Health. Sep 11, 2018. doi:10.1177/1941738118799084
Hansel J, Burgstahler C, Nieß AM. Diagnostische und therapeutische Pfade bei Sportlern mit Verdacht auf Myokarditis – eine Registerstudie. Dtsch Z Sportmed. 2014; 65: 50-54. doi:10.5960/dzsm.2012.046
Laszlo R, Scharhag J, Burgstahler C, Striegel H, Steinacker JM. Sportkardiologie. Überblick über relevante klinische Themen. Herz. 2018; 43: 53–60. doi:10.1007/s00059-016-4521-6
Riding NR, Drezner JA. Performance of the BMJ learning training modules for ECG interpretation in athletes. Heart. 2018; 104(24): 2051–2057. doi:10.1136/heartjnl-2018-313066