Gendoping bald auch bei Sportlern?
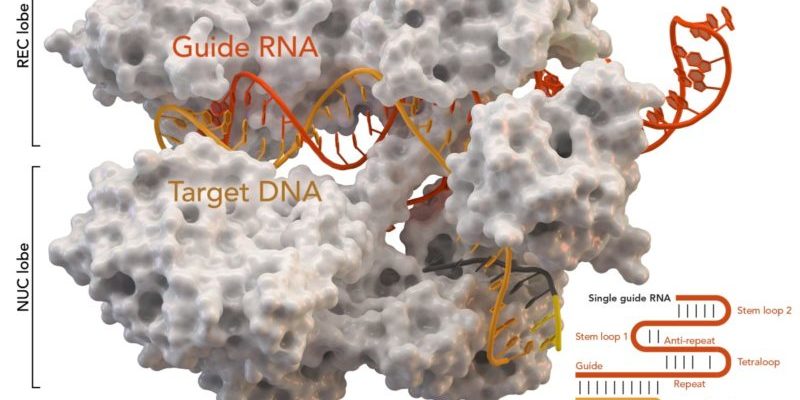
Eine chinesische Gruppe von Wissenschaftlern publizierte vor einem Jahr einen Bericht über Hunde mit der doppelten Muskelmenge normaler Beagles. Mithilfe der CRISP/Cas9-Technik wurde den Tieren das Myostatin-Gen entfernt, welches das Wachstum der Muskulatur kontrolliert (1). In der Zwischenzeit sind auch Mäuse, Ratten, Ziegen, Schweine, Schafe und Affen »entwickelt« worden, deren Erbgut mit CRISPR/Cas9 modifiziert wurde. Bei Tieren funktioniert die Methode bereits recht zuverlässig, wenngleich die Erfolge nicht darüber hinweg täuschen sollen, dass bei der Gen-Editierung mittels CRISPR/Cas9 viel »Ausschuss« produziert wird. Bei humanen Zellen gelingt es in etwa fünf Prozent der Fälle, ein Gen gezielt auszuschalten. Soll ein Gen repariert werden, liegt die Erfolgsquote bei nur ein bis zwei Prozent. Nichtsdestotrotz arbeiten Wissenschaftler weltweit daran, die präzise, technisch einfache, schnell anzuwendende und dadurch kostengünstige Gen-Editierungsmethode auch für die Behandlung menschlicher Erkrankungen, die durch Gendefekte hervorgerufen werden, nutzen zu können.
Gendoping durch CRISPR/Cas9?
Was eine bislang einzigartige Therapiemethode für kranke Menschen werden könnte, hat aber theoretisch auch das Potenzial, die körperlichen Voraussetzungen von Sportlern zu verändern. Die Welt-Anti-Doping-Agentur (WADA) definiert diese Form des Dopings, das Gendoping, als »den nichttherapeutischen Gebrauch von Zellen, Genen und genetischen Elementen sowie die Beeinflussung der Genexpression mit der Möglichkeit, die Leistungsfähigkeit zu steigern.« Interessant ist die Methode für Dopingwillige dadurch, dass die Veränderungen im Genom sich nicht von der natürlichen Struktur unterscheiden. Das bedeutet eine ganz neue Herausforderung für den Dopingnachweis. Interessant ist ebenfalls, dass gleichzeitig mehrere Gene/Genorte verändert werden können. Ein Muskelwachstum durch Herunterregulation von Myostatin, wie bei den chinesischen Beagles, könnte in Kraftsportarten interessant sein, eine Manipulation des EPO-Gens für Ausdauerathleten.
Welche Risiken durch die genetische Veränderung entstehen können, ist zum jetzigen Zeitpunkt ebenso unklar wie der tatsächliche Nutzen. Denn die meisten sportlichen Fähigkeiten sind – soweit heute bekannt – nicht auf einzelne Gene, sondern auf eine günstige Konstellation vieler Parameter zurückzuführen. Auch der Einfluss epigenetischer Regulationsmechanismen auf die Leistungsfähigkeit ist noch zu wenig verstanden, um gezielt eingreifen zu können. Durch diese wissenschaftliche Innovation erhält das Thema Gendoping jedoch sicherlich neue Schubkraft.